中华人民共和国农业农村部公报第332号
根据《兽药管理条例》和《兽药注册办法》规定,经审查,批准百美达美国生产厂生产的阿莫西林注射液在我国注册,核发《进口兽药注册证书》,并发布产品质量标准、说明书、标签和残留检测方法标准(试行),自发布之日起执行。
批准法国诗华动物保健公司生产的马波沙星注射液在我国再注册,核发《进口兽药注册证书》,并发布修订后的产品质量标准、说明书、标签和每日允许摄入量及最高残留限量标准(试行),自发布之日起执行。此前发布的该产品兽药质量标准、说明书和标签同时废止。
批准勃林格殷格翰动物保健(美国)有限公司St.Joseph生产厂生产的副猪嗜血杆菌病灭活疫苗(12型Z-1517株)在我国再注册,核发《进口兽药注册证书》,并发布修订后的产品质量标准、说明书和标签,自发布之日起执行。此前发布的该产品兽药质量标准、说明书和标签同时废止。
批准Labiana生命科学制药厂等2家公司生产的美洛昔康注射液等2种兽药产品在我国变更注册,并发布变更后的产品质量标准、说明书和标签,自发布之日起执行。此前发布的该产品兽药质量标准、说明书和标签同时废止。
批准修订完善农业农村部公告第283号中的莫能菌素预混剂质量标准、说明书和标签,并发布完善后的产品质量标准、说明书和标签,自发布之日起执行。此前发布的该产品兽药质量标准、说明书和标签同时废止。
特此公告。
附件:1.进口兽药注册目录
2.质量标准
3.说明书和标签
4. 阿莫西林残留检测方法标准(试行)
5. 马波沙星的每日允许摄入量和最高残留限量(试行)
农业农村部
2020年9月7日
附件1
进口兽药注册目录
|
兽药名称 |
生产厂名称 |
国 别 |
进口兽药 注册 证书号 |
有效期限 |
备注 |
|
阿莫西林注射液 (100ml∶15g) Amoxicillin Injection (100ml∶15g) |
百美达美国生产厂 Constant Irwindale Inc. |
美国 |
(2020) 外兽药证字 38号 |
2020.09.07 — 2025.09.06 |
注册 |
|
阿莫西林注射液 (250ml∶37.5g) Amoxicillin Injection (250ml∶37.5g) |
(2020) 外兽药证字 39号 |
||||
|
马波沙星注射液 (50ml∶5g) Marbofloxacin Injection (50ml∶5g) |
法国诗华动物保健公司 CEVA SANTE ANIMALE S.A. |
法国 |
(2020) 外兽药证字 40号 |
2020.09.07 — 2025.09.06 |
再注册 |
|
马波沙星注射液 (100ml∶10g) Marbofloxacin Injection (100ml∶10g) |
(2020) 外兽药证字 41号 |
||||
|
马波沙星注射液 (250ml∶25g) Marbofloxacin Injection (250ml∶25g) |
(2020) 外兽药证字 42号 |
||||
|
副猪嗜血杆菌病灭活疫苗(12型Z-1517株) Haemophilus parasuis Vaccine,Inactivated(Serotype 12 Strain Z-1517) |
勃林格殷格翰动物保健(美国)有限公司St.Joseph生产厂 Boehringer Ingelheim Animal Health USA Inc. |
美国 |
(2020) 外兽药证字 43号 |
2020.09.07 — 2025.09.06 |
再注册 |
|
美洛昔康注射液 Meloxicam Injection |
Labiana生命科学制药厂 Labiana Life Sciences S.A. |
西班牙 |
(2018) 外兽药证字 57号 |
2018.12.19 — 2023.12.18 |
变更注册:增加新的适应症(缓解犊牛去角操作后疼痛) |
|
(2018) 外兽药证字 58号 |
|||||
|
(2018) 外兽药证字 59号 |
|||||
|
(2018) 外兽药证字 60号 |
|||||
|
注射用血促性素绒促性素 Serum Gonadotrophin and Chorionic Gonadotrophin for Injection |
英特威国际有限公司 Intervet International B.V. |
荷兰 |
(2016) 外兽药证字 16号 |
2016.05.06 — 2021.05.05 |
变更注册:增加宁波人健药业集团股份有限公司为绒促性素的原料药供应商、修改质量标准 |
|
莫能菌素预混剂 Monensin Premix |
美国礼蓝动物保健有限公司美国生产厂 Elanco Clinton Laboratories |
美国 |
(2020) 外兽药证字 08号 |
2020.03.23 — 2025.03.22 |
完善质量标准、说明书和标签 |
附件2略
附件3
阿莫西林注射液等6种兽药产品说明书和标签
一、 阿莫西林注射液说明书和标签
(一)阿莫西林注射液说明书
兽用处方药
【兽药名称】
通用名称:阿莫西林注射液
商品名称:百莫林®(Bimoxyl® LA)
英文名称:Amoxicillin Injection
汉语拼音:AmoxilinZhusheye
【主要成分】阿莫西林。
【性状】本品为细微颗粒的混悬油溶液。静置后,细微颗粒下沉,摇匀后成均匀的类白色混悬液。
【药理作用】药效学β-内酰胺类抗生素。阿莫西林通过抑制细菌细胞壁的合成而发挥杀菌作用,可使细菌迅速成为球状体而溶解、破裂。对链球菌属、不产青霉素酶葡萄球菌等革兰氏阳性菌和不产青霉素酶的大肠埃希氏菌、沙门氏菌属、嗜血杆菌、克雷伯氏菌、巴氏杆菌等革兰氏阴性菌具有良好的抗菌活性。
药动学牛和猪肌内注射以及犬皮下注射本品后吸收迅速,0.5~3小时血药峰浓度达峰值1.5~4.5µg/ml。生物利用度为85%~100%。重复注射(2次注射间隔48小时)后药代动力学参数稳定,无蓄积效应,主要以活性形式经由肾脏排泄。
药物相互作用 1.本品与氨基糖苷类合用,可提高后者在菌体内的浓度,呈现协同作用;2.大环内酯类、四环素类和胺酰醇类等快效抑菌剂对本品有干扰作用,不宜合用。
【适应证】牛:用于治疗和控制对阿莫西林敏感的革兰氏阳性菌和革兰氏阴性菌感染。猪和犬:用于治疗对阿莫西林敏感的感染性疾病。
【用法与用量】以阿莫西林计。牛和猪肌内注射、犬皮下注射:一次量,每1kg体重,牛、猪和犬15mg,如需要可在48小时再注射一次。每个注射位点的最大注射体积:牛20ml;猪5ml;犬2.5ml。
【不良反应】本品给药后可能出现过敏反应,偶尔出现严重过敏反应(如过敏性休克)。注射部位偶见一过性反应。
【注意事项】 1.禁用于有β-内酰胺类抗生素过敏史的动物。
2.禁止静脉注射和鞘内注射。
3.怀孕期和妊娠期动物慎用。
4.使用前摇匀。
5.使用干燥、无菌的针头和注射器抽取,每次抽取前应擦拭瓶盖。
6.已用或未用完的产品均需进行安全处置。
7.已知对β-内酰胺类抗生素过敏者应避免接触本品。如不慎与皮肤或眼睛接触,立即用大量水冲洗。注射、吸入、内服或皮肤接触β-内酰胺类抗生素均可引起过敏反应,如接触本品后出现皮疹等症状,需就医;如出现面部、嘴唇或眼睛肿胀或呼吸困难等严重症状,需进行紧急医疗处理。
8.如果发生任何严重的不良反应或包装说明上未提及的不良反应,应及时通知兽医。
【休药期】牛18日,弃奶期72小时;猪21日。
【规格】(1)100ml∶15g (2)250ml∶37.5g
【包装】
【贮藏】密闭,25℃以下干燥处保存。
【有效期】 24个月;开启后常温保存28日。
【进口兽药注册证号】
【生产企业】百美达美国生产厂(Constant Irwindale Inc.)
地址:5539 Ayon Avenue, Irwindale, California, 91706, USA
(二)阿莫西林注射液标签
兽用处方药
【兽药名称】
通用名称:阿莫西林注射液
商品名称:百莫林®(Bimoxyl® LA)
英文名称:Amoxicillin Injection
汉语拼音:AmoxilinZhusheye
【主要成分】阿莫西林。
【性状】本品为细微颗粒的混悬油溶液。静置后,细微颗粒下沉,摇匀后成均匀的类白色混悬液。
【适应证】牛:用于治疗和控制对阿莫西林敏感的革兰氏阳性菌和革兰氏阴性菌感染。猪和犬:用于治疗对阿莫西林敏感的感染性疾病。
【用法与用量】以阿莫西林计。牛和猪肌内注射、犬皮下注射:一次量,每1kg体重,牛、猪和犬15mg,如需要可在48小时再注射一次。每个注射位点的最大注射体积:牛20ml;猪5ml;犬2.5ml。
【规格】(1)100ml∶15g (2)250ml∶37.5g
【进口兽药注册证号】
【生产日期】
【生产批号】
【有效期】至
【休药期】牛18日,弃奶期72小时;猪21日。
【贮藏】密闭,25℃以下干燥处保存。
【包装】
【生产企业】百美达美国生产厂(Constant Irwindale Inc.)
地址:5539 Ayon Avenue, Irwindale, California, 91706, USA
二、马波沙星注射液说明书和标签
(一)马波沙星注射液说明书
兽用处方药
【兽药名称】
通用名称:马波沙星注射液
商品名称:牧康欣Ò(Marbox®)
英文名称:Marbofloxacin Injection
汉语拼音:Maboshaxing Zhusheye
【主要成分】 马波沙星
【性状】 本品为黄色澄明液体。
【药理作用】 药效学 马波沙星是动物专用的氟喹诺酮类抗菌药。主要通过抑制细菌脱氧核糖核酸回旋酶A亚基的活性而抑制细菌DNA复制、转录及蛋白质的合成。马波沙星抗菌谱广,对革兰氏阳性菌(特别是葡萄球菌属)、革兰氏阴性菌(大肠杆菌、多杀性巴斯德杆菌、溶血性曼氏杆菌、睡眠嗜组织菌、鼠伤寒沙门氏菌、空肠弯曲杆菌、费氏柠檬酸杆菌、阴沟肠杆菌、粘质沙雷氏菌、摩氏摩根氏菌、变形杆菌、志贺菌属、猪胸膜肺炎放线杆菌、支气管败血性鲍特氏菌、克雷伯菌属、嗜血杆菌属等)及支原体有效。
药动学 动物注射马波沙星吸收迅速而完全,血浆蛋白结合率低,生物利用度接近100%。猪肌内注射马波沙星2mg/kg,约1小时血药浓度即可达峰值,Cmax约为1.7µg/ml。牛肌内单次注射马波沙星8mg/kg,约1 小时血药浓度可达到峰值,Cmax约8µg/ml;牛皮下注射马波沙星2mg/kg后,约1小时血药浓度可达到峰值,Cmax约1.7µg/ml。马波沙星广泛分布于肝、肾、皮肤、肺、膀胱等组织,在大部分组织内的药物浓度高于血药浓度。马波沙星在猪体内的消除半衰期为8.7小时,牛肌内注射消除半衰期为9.5小时,牛皮下注射消除半衰期为5.6小时,主要以原形经尿和粪便排泄。
【适应证】 用于治疗由敏感菌引起的母猪子宫炎-乳腺炎-无乳综合征,由牛呼吸道感染和牛泌乳期乳腺炎。
【用法与用量】 以马波沙星计。
母猪子宫炎-乳腺炎-无乳综合征:肌内注射。一次量,每1kg体重2mg(即每50kg体重1ml),一日1次,连用3日。
牛呼吸道感染:肌内注射。一次量,每1 kg体重8mg(即每25kg体重2ml),单次注射。同一部位使用不得超过20ml。
牛泌乳期乳腺炎:皮下注射。一次量,每1kg体重 2mg(即每50kg体重1ml),一日1次,连用3日。
【不良反应】 本品可能会引起注射部位短暂的刺激反应。
【注意事项】
1. 仅在兽医指导下使用。
2. 猪、牛推荐颈部肌内注射。
3. 对马波沙星或其他喹诺酮类药物过敏的动物禁用。
4. 已知对喹诺酮类药物耐药的菌株或疑似耐药菌株感染的动物禁用。
5. 对喹诺酮类药物过敏的人员避免接触本品。
6. 如果不慎与皮肤或眼睛接触,立即用大量水进行冲洗。
7. 瓶塞最多可穿刺45次,应选择合适的包装规格。
【休药期】 猪4日;牛:肌内注射3日,弃奶期72小时;牛:皮下注射6日,弃奶期36小时。
【规格】 按C17H19FN4O4计算 (1)50ml∶5g (2)100ml∶10g (3)250 ml∶25g
【包装】
【贮藏】 遮光,密闭保存。
【有效期】 36个月;开启后28日。
【进口兽药注册证号】
【生产企业】 法国诗华动物保健公司(CEVA SANTE ANIMALE S.A.)
地址:10 AVENUE DE LA BALLASTIERE,33500 LIBOURNE,FRANCE
(二)马波沙星注射液标签
兽用处方药
【兽药名称】
通用名称:马波沙星注射液
商品名称:牧康欣Ò(MarboxÒ)
英文名称:Marbofloxacin Injection
汉语拼音:Maboshaxing Zhusheye
【主要成分】 马波沙星
【性状】 本品为黄色澄明液体。
【适应证】 用于治疗由敏感菌引起的母猪子宫炎-乳腺炎-无乳综合征,由牛呼吸道感染和牛泌乳期乳腺炎。
【用法与用量】 以马波沙星计。
母猪子宫炎-乳腺炎-无乳综合征:肌内注射。一次量,每1kg体重2mg(即每50kg体重1ml),一日1次,连用3日。
牛呼吸道感染:肌内注射。一次量,每1kg体重8mg(即每25kg体重2ml),单次注射。同一部位使用不得超过20ml。
牛泌乳期乳腺炎:皮下注射。一次量,每1kg体重 2mg(即每50kg体重1ml),一日1次,连用3日。
【规格】 按C17H19FN4O4计算 (1)50ml ∶5g (2)100ml∶10g (3)250ml∶25g
【进口兽药注册证号】
【生产日期】
【生产批号】
【有效期】至
【休药期】 猪4日;牛:肌内注射3日,弃奶期72小时;牛:皮下注射6日,弃奶期36小时。
【包装】
【贮藏】 遮光,密闭保存。
【生产企业】 法国诗华动物保健公司(CEVA SANTE ANIMALE S.A.)
地址:10 AVENUE DE LA BALLASTIERE, 33500 LIBOURNE, FRANCE
三、副猪嗜血杆菌病灭活疫苗(12型Z-1517株)说明书和内包装标签
(一)副猪嗜血杆菌病灭活疫苗(12型Z-1517株)说明书
兽用
【兽药名称】
通用名 副猪嗜血杆菌病灭活疫苗(12型Z-1517株)
商品名 无
英文名 Haemophilus parasuis Vaccine,Inactivated(Serotype 12 Strain Z-1517)
汉语拼音 Fuzhushixueganjunbing Miehuoyimiao(12 Xing Z-1517 Zhu)
【主要成分与含量】 疫苗中含有灭活的12型副猪嗜血杆菌,灭活前含活菌至少1.5×109个/头份。
【性状】 白色不透明混悬液。
【作用与用途】 用于预防由副猪嗜血杆菌引起的副猪嗜血杆菌病。免疫期为132日。
【用法与用量】 肌肉注射。3周龄以上的猪,每头2ml。种猪,每6个月重复免疫接种疫苗一次。
【不良反应】 本品接种后可能会发生过敏反应,可使用肾上腺素进行治疗。
【注意事项】 (1)疫苗切勿冻结。
(2)用前充分摇匀,一旦打开,应尽快用完。
(3)屠宰前60日禁用。
【规格】 (1)100ml(50头份)/瓶 (2)500ml(250头份)/瓶
【包装】 1瓶/盒
【贮藏与有效期】 2~8℃保存,有效期为36个月。
【《进口兽药注册证书》证号】
【生产企业】 勃林格殷格翰动物保健(美国)有限公司(St.Joseph生产厂)(Boehringer Ingelheim Animal Health USA Inc.)
地址:2621 North Belt Highway St.Joseph,MO 64506 U.S.A.
仅在兽医指导下使用
(二)副猪嗜血杆菌病灭活疫苗(12型Z-1517株)内包装标签
兽用
副猪嗜血杆菌病灭活疫苗(12型Z-1517株)
100(500)ml/瓶
《进口兽药注册证书》证号:
批 号:
生产日期:
【作用与用途】 用于预防由副猪嗜血杆菌引起的副猪嗜血杆菌病。免疫期为132日。
【用法与用量】 肌肉注射。3周龄以上的猪,每头2ml。种猪,每6个月重复免疫接种疫苗一次。
【注意事项】 疫苗切勿冻结;用前充分摇匀,一旦打开,应尽快用完;屠宰前60日禁用;本品接种后可能会发生过敏反应,可使用肾上腺素进行治疗。
【贮藏与有效期】 2~8℃保存,有效期为36个月。
【生产企业】 勃林格殷格翰动物保健(美国)有限公司(St.Joseph生产厂)(Boehringer Ingelheim Animal Health USA Inc.)地址:2621 North Belt Highway St.Joseph,MO 64506 U.S.A.
仅在兽医指导下使用
四、美洛昔康注射液说明书和标签
(一)美洛昔康注射液说明书
兽用处方药
【兽药名称】
通用名称:美洛昔康注射液
商品名称:美达佳
英文名称:Meloxicam Injection
汉语拼音:MeiluoxikangZhusheye
【主要成分】美洛昔康
【性状】本品为黄色澄明液体。
【药理作用】非甾体类抗炎药。美洛昔康通过抑制前列腺素的合成发挥作用,主要功能为抗炎、镇痛和解热。美洛昔康可抑制白细胞向发炎组织的趋化作用,轻度抑制胶原蛋白诱导的血小板聚集。另外,在犊牛、泌乳牛和猪使用美洛昔康时,显示美洛昔康具有抗内毒素作用,可抑制大肠杆菌内毒素诱导生成血栓素B2。
【适应证】牛:配合适宜的抗菌药使用,辅助治疗急性呼吸道感染以缓解牛的临床症状;辅助治疗急性乳房炎;缓解犊牛去角操作后疼痛。配合内服补液使用,辅助治疗腹泻以缓解超过一周龄的犊牛与青年非泌乳牛的临床症状。
猪:用于跛行与炎症以减轻患猪非感染性运动异常的症状;配合适宜的抗菌药使用,辅助治疗产后败血症与毒血症(乳房炎-子宫炎-无乳综合症)。
【用法与用量】以美洛昔康计。牛皮下或静脉注射:配合适宜的抗菌药或内服补液使用,一次量,每1kg体重,牛0.5mg,仅用一次。
猪肌内注射:配合适宜的抗菌药使用,一次量,每1kg体重,猪0.4mg。若需要,24小时之后,再注射一次。
【不良反应】1.牛皮下注射或猪肌内注射本品后,注射部位偶见(<10%)轻微的一过性肿胀。
2.有极少数动物出现过敏反应,应对症治疗。
【注意事项】1.禁用于肝功能、心功能或肾功能损伤、出血异常,或胃肠道溃疡的动物。
2.禁用于对本品过敏的动物。
3.禁用于治疗一周龄以内的犊牛腹泻。
4.具有潜在肾毒性,慎用于严重脱水、血容量减少或低血压等需要注射补液的动物。
5.禁与糖皮质激素、其他非甾体类抗炎药或抗凝血剂合用。
6.在犊牛去角操作前20分钟使用本品,可减轻去角操作后疼痛。单独使用本品不能提供足够的疼痛缓解效果。在去角操作中,可配合适宜的麻醉剂或镇静剂使用,以减轻疼痛。
7.对NSAIDs过敏的人应该避免接触本品。
8.置于儿童不可触及处。
【休药期】牛15日,猪5日;弃奶期5日。
【规格】(1)20ml∶400mg (2)50ml∶1g (3)100ml∶2g (4)250ml∶5g
【包装】
【贮藏】密闭保存。
【有效期】36个月;开启后28日。
【进口兽药注册证号】
【生产企业】Labiana生命科学制药厂(Labiana Life Sciences S.A.)
地址:Venus 26, Can Parellada Industrial, 08228 Terrassa, Barcelona, Spain
(二)美洛昔康注射液标签
兽用处方药
【兽药名称】
通用名称:美洛昔康注射液
商品名称:美达佳
英文名称:Meloxicam Injection
汉语拼音:MeiluoxikangZhusheye
【主要成分】美洛昔康
【适应证】牛:配合适宜的抗菌药使用,辅助治疗急性呼吸道感染以缓解牛的临床症状;辅助治疗急性乳房炎;缓解犊牛去角操作后疼痛。配合内服补液使用,辅助治疗腹泻以缓解超过一周龄的犊牛与青年非泌乳牛的临床症状。
猪:用于跛行与炎症以减轻患猪非感染性运动异常的症状;配合适宜的抗菌药使用,辅助治疗产后败血症与毒血症(乳房炎-子宫炎-无乳综合症)。
【用法与用量】以美洛昔康计。牛皮下或静脉注射:配合适宜的抗菌药或内服补液使用,一次量,每1kg体重,牛0.5mg,仅用一次。
猪肌内注射:配合适宜的抗菌药使用,一次量,每1kg体重,猪0.4mg。若需要,24小时之后,再注射一次。
【休药期】牛15日,猪5日;弃奶期5日。
【规格】(1)20ml∶400mg (2)50ml∶1g (3)100ml∶2g (4)250ml∶5g
【包装】
【生产日期】
【生产批号】
【有效期】至
【贮藏】密闭保存。
【生产企业】Labiana生命科学制药厂(Labiana Life Sciences S.A.)
地址:Venus 26, Can Parellada Industrial, 08228 Terrassa, Barcelona, Spain
五、注射用血促性素绒促性素说明书和标签
(一)注射用血促性素绒促性素说明书
兽用
【兽药名称】
通用名称:注射用血促性素绒促性素
商品名称:PG600,必精600
英文名称:Serum Gonadotrophin and Chorionic Gonadotrophin for Injection
汉语拼音:Zhusheyong Xuecuxingsu Rongcuxingsu
【主要成分】 血促性素、绒促性素
【性状】 本品为白色或类白色冻干块状物或粉末。
【药理作用】 激素类药。本品具有促卵泡素(FSH)和促黄体素(LH)样作用。对母畜可促进卵泡成熟、排卵和黄体生成,并刺激黄体分泌孕激素。对未成熟卵泡无作用。对公畜可促进睾丸间质细胞分泌雄激素,促使性器官、副性征的发育、成熟,使隐睾病畜的睾丸下降,并促进精子生成。
【适应证】 具有促进卵泡成熟和排卵作用。用于缩短经产母猪和初产母猪的发情间隔,控制同步发情。
【用法与用量】 用5ml或25ml的磷酸盐缓冲液溶解1头份或5头份的冻干产品。母猪耳后颈部肌肉、皮下注射:一次量,5ml /头。
【不良反应】 本产品属于蛋白质激素,注射后偶见速发的过敏反应。首次出现过敏症状后给予肾上腺素(1:1000),静脉注射剂量为2~3ml,肌肉注射为2~8ml。
【注意事项】 1. 在初级黄体期或发情中期给药会促进卵巢囊肿的发生。
2. 妊娠母猪、促性腺激素过敏的母猪禁用。
3. 禁止超剂量使用。
4. 用磷酸盐缓冲液溶解后的溶液不宜贮存;和其他药物一起使用可能会影响繁殖。
【休药期】 不需要制定。
【规格】 (1)PMSG 400 IU + hCG 200 IU + 注射用磷酸盐缓冲液5ml(1头份)
(2)PMSG 2000 IU + hCG 1000 IU + 注射用磷酸盐缓冲液25ml(5头份)
【包装】 1头份×5/盒;5头份×1/盒。
【贮藏】 在2~8℃冰箱保存。溶解后的冻干产品于2~8℃保存,可保存24小时。
【有效期】 36个月。
【进口兽药注册证号】
【生产企业】 英特威国际有限公司(Intervet International B.V.)
地址:Wim de Körverstraat 35, 5831AN BOXMEER, Holland
(二)注射用血促性素绒促性素标签
兽用
【兽药名称】
通用名称:注射用血促性素绒促性素
商品名称:PG600,必精600
英文名称:Serum Gonadotrophin and Chorionic Gonadotrophin for Injection
汉语拼音:Zhusheyong Xuecuxingsu Rongcuxingsu
【主要成分】 血促性素、绒促性素
【适应证】 具有促进卵泡成熟和排卵作用。用于缩短经产母猪和初产母猪的发情间隔,控制同步发情。
【用法与用量】 用5ml或25ml的磷酸盐缓冲液溶解1头份或5头份的冻干产品。母猪耳后颈部肌肉、皮下注射:一次量,5ml /头(PMSG 400 IU+hCG 200 IU)。
【规格】 (1)PMSG 400 IU + hCG 200 IU + 注射用磷酸盐缓冲液5ml (1头份)
(2)PMSG 2000 IU + hCG 1000 IU + 注射用磷酸盐缓冲液25ml (5头份)
【进口兽药注册证号】
【生产日期】
【生产批号】
【有效期】至
【休药期】 不需要制定。
【贮藏】 在2~8℃冰箱保存。溶解后的冻干产品于2~8℃保存,可保存24小时。
【包装】 1头份×5/盒(或5头份×1/盒)
【生产企业】 英特威国际有限公司(Intervet International B.V.)
地址:Wim de Körverstraat 35, 5831AN BOXMEER, Holland
六、莫能菌素预混剂说明书和标签
(一)莫能菌素预混剂说明书
兽用
【兽药名称】
通用名称:莫能菌素预混剂
商品名称:欲可胖® 200(Elancoban® 200)
英文名称:Monensin Premix
汉语拼音:Monengjunsu Yuhunji
【主要成分】 莫能菌素
【性状】 本品为黄褐色粉末。
【药理作用】 抗生素类药。本品为广谱抗球虫药,对鸡柔嫩、毒害、巨型、和缓、布氏和堆型艾美耳球虫都有效。莫能菌素与钠、钾离子有特殊的亲和力,可形成亲脂性络合物,透过球虫生物膜,使球虫体内钠离子量急剧增加,妨碍离子的正常平衡和运转,球虫体内过剩的钠离子不能排出,最后使虫体膨胀而死亡。此外,莫能菌素能调节瘤胃微生物发酵类型,提高发酵物中丙酸的比例,从而提高饲料的能量利用率;节省离子在组织和细胞间运输的能量消耗;抑制瘤胃微生物产生乳酸的活性,从而防止高精料育肥的情况下可能发生的酸中毒。
【适应证】 用于防治鸡球虫病;辅助缓解奶牛酮病症状,提高产奶量。
【用法与用量】 以莫能菌素计。用于防治鸡球虫病,混饲:每1000kg饲料,鸡90~110g。辅助缓解奶牛酮病症状,混饲:奶牛(泌乳期),一日量,每头150~450mg。
【不良反应】
1.饲料中添加量超过120mg/kg时,可引起鸡增长率和饲料转化率下降。
2.超剂量使用莫能菌素时,可导致牛增重率下降,甚至中毒死亡。
3.饲喂前必须将莫能菌素与饲料混匀,禁止直接饲喂未经稀释的莫能菌素。
【注意事项】
1.10周龄以上火鸡、珍珠鸡及鸟类对本品较敏感,不宜应用;超过16周龄的鸡禁用。
2.马属动物禁用。
3.禁止与泰妙菌素、竹桃霉素同时使用,以免发生中毒。
4.搅拌配料时防止与人的皮肤、眼睛接触。
5.蛋鸡产蛋期禁用。
6.本品用于防治鸡球虫病时可在商品饲料和养殖过程中使用。
【休药期】 鸡5日。
【规格】 100g:20g(2000万单位)
【包装】
【贮藏】 密闭,在干燥处保存。
【有效期】 24个月。
【进口兽药注册证号】
【生产企业】 美国礼蓝动物保健有限公司美国生产厂(Elanco Clinton Laboratories)
地址:10500 South State Road 63, Clinton, Indiana, 47842-0099, U.S.A.
(二)莫能菌素预混剂标签
兽用
【兽药名称】
通用名称:莫能菌素预混剂
商品名称:欲可胖® 200(Elancoban® 200)
英文名称:Monensin Premix
汉语拼音:Monengjunsu Yuhunji
【主要成分】 莫能菌素
【性状】 本品为黄褐色粉末。
【适应证】 用于防治鸡球虫病;辅助缓解奶牛酮病症状,提高产奶量。
【用法与用量】 以莫能菌素计。用于防治鸡球虫病,混饲:每1000kg饲料,鸡90~110g。辅助缓解奶牛酮病症状,混饲:奶牛(泌乳期),一日量,每头150~450mg。
【规格】100g:20g(2000万单位)
【进口兽药注册证号】
【生产日期】
【生产批号】
【有效期】至
【休药期】 鸡5日;蛋鸡产蛋期禁用。
【贮藏】 密闭,在干燥处保存。
【包装】
【生产企业】 美国礼蓝动物保健有限公司美国生产厂(Elanco Clinton Laboratories)
地址:10500 South State Road 63, Clinton, Indiana, 47842-0099, U.S.A.
附件4
阿莫西林残留检测方法标准(试行)
动物性食品中阿莫西林残留量的测定
液相色谱-串联质谱法
1 范围
本标准规定了动物性食品中阿莫西林残留检测的制样和液相色谱-串联质谱法测定方法。
本标准适用于牛的肝脏、肾脏及脂肪中阿莫西林残留量的检测。
2 规范性引用文件
下列文件中的条款通过本标准的引用而成为本标准的条款。凡是注日期的引用文件,仅注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB/T 6682 分析实验室用水规格和试验方法
3 原理
试料中残留的阿莫西林用水和提取,乙腈饱和的正己烷溶液除脂,C18固相萃取柱净化,用液相色谱-串联质谱法测定,外标法定量。
4 试剂或材料
以下所用的试剂,除特别注明外均为分析纯;水为符合GB/T 6682中规定的一级水。
4.1 阿莫西林对照品(C16H19N3O5S),含量86.6%。
4.2 C18固相萃取柱,如Agilent- C18(200 mg/3mL)或效能相当者。
4.3 乙腈色谱纯
4.4 正己烷色谱纯
4.5 甲酸色谱纯
4.6 乙腈饱和的正己烷溶液:取50mL乙腈和450mL正己烷置于500mL试剂瓶中,超声混匀备用。
4.7 阿莫西林储备液(1mg/mL):准确称取阿莫西林对照品5.0mg,置于5mL容量瓶内,用水溶解并稀释至刻度,摇匀即得。-20oC冰箱中保存,有效期1个月。
4.8 阿莫西林系列标准工作液的配制:准确量取阿莫西林储备液1mL置于10mL容量瓶中,用水溶解并稀释至刻度,稀释成浓度为100µg/mL的工作液,再依次稀释至浓度为0.05、0.1、0.25、0.5、1、2µg/mL的标准工作液,4℃贮藏,有效期5天。
5 仪器设备
5.1 高效液相色谱-串联质谱仪配有电喷雾离子源。
5.2 固相萃取装置
5.3 多管涡旋振荡器
5.4 分析天平感量0.01g。
5.4 天平感量0.0001g。
5.5 氮吹仪
5.6 冷冻高速离心机
5.7 微孔水相滤头 0.22μm孔径。
6 试样的制备与保存
6.1 试料的制备
取适量新鲜或解冻的空白或供试组织,绞碎,并使均质。
——取均质的供试样品,作为供试试样。
——取均质的空白样品,作为空白试样。
——取均质的空白样品,添加适宜浓度的标准工作液,作为空白添加试样。
6.2 试料的保存
-20℃以下保存。
7 试验步骤
7.1 提取
准确称取(2.0±0.05)g试样,置于50mL离心管中,精密加水2mL,涡旋混匀,再精密加入乙腈8mL,900r/min振荡10min,10000r/min离心10min。将上清液转移至50mL离心管中,加入乙腈饱和的正己烷溶液5mL,900r/min振荡5min,10000r/min离心5min,去除上层正己烷层,取下层清液待上柱净化。
7.2 净化
依次用乙腈5mL、水5mL活化C18固相萃取柱,取全部备用液过柱,收集流出液置15mL离心管内,样品液全部流出后,挤干固相萃取柱。流出液于40℃下氮吹吹至1.5mL,用水定容至2mL,900r/min振荡5min,10000 r/min离心5min,过滤膜,待测。
7.3 基质匹配标准曲线的配制
取牛肝脏、肾脏和脂肪空白样品,按7.1和7.2项下方法进行处理后,制得基质空白溶液,分别精密量取系列阿莫西林标准工作液100μL,加入到空白基质溶液900μL中,制得5、10、25、50、100、200μg/L系列基质匹配标准溶液,供高效液相色谱-串联质谱测定。以测得的阿莫西林特征离子峰面积作为纵坐标,对应的浓度为横坐标,绘制标准曲线。求线性回归方程和相关系数。
7.4 测定
7.4.1 色谱参考条件
色谱柱:C18色谱柱,2.1mm×50mm,1.7µm或效能相当者。
流动相:A相为0.1%甲酸溶液;B相为乙腈。
流速:0.3mL/min。
柱温:40℃。
进样体积:5μL。
梯度洗脱:梯度洗脱程序见表1。
表1 梯度洗脱条件
|
时间(min) |
流动性A(%) |
流动性B(%) |
|
0.0 |
90 |
10 |
|
2.0 |
90 |
10 |
|
2.5 |
5 |
95 |
|
5.0 |
5 |
95 |
|
5.1 |
90 |
10 |
|
7.0 |
90 |
10 |
7.4.2 质谱参考条件
离子源:电喷雾离子源ESI(+)。
干燥气温度(Gas Temp):250℃;
干燥气流量(Gas Flow):7L/min;
雾化气压力(Nebulier):50psi;
鞘气温度(Sheath Gas Temp):300℃;
鞘气流量(Sheath Gas Flow):11L/min;
毛细管电压(Capillary):3500V;
喷嘴电压(Nozzle Voltage):1000V;
电晕电流(Corona Current):0.64μA。
定性定量离子对及锥孔电压、碰撞能量对见表2。
表2 定性定量离子及锥孔电压、碰撞能量的参考值
|
药物 |
定性离子对 |
定量离子对 |
锥孔电压(V) |
碰撞能量 |
|
(m/z) |
(m/z) |
|
(eV) |
|
|
阿莫西林 |
366.0>349.1 |
366.0>349.1 |
90 |
5 |
|
366.0>208.2 |
10 |
7.4.3 定性测定
通过试样溶液色谱图的保留时间与基质匹配标准溶液色谱图的保留时间、各色谱峰的特征离子与相应浓度标准溶液色谱峰的特征离子相对照定性。试样溶液与基质匹配标准溶液色谱峰的保留时间的相对偏差不大于5%;试样特征离子的相对丰度与浓度相当标准溶液中对应的相对丰度进行比较,若相对丰度偏差不超过表3的规定,则可判断样品中存在相应的被测物。
表3 定性测定时相对离子丰度的最大允许偏差
|
相对离子丰度 |
>50% |
>20%至50% |
>10%至20% |
≤10% |
|
允许的相对偏差 |
±20% |
±25% |
±30% |
±50% |
7.4.4 定量测定
取空白试样溶液和相应的标准工作液,配制基质匹配标准曲线,实测试样采用单点或多点校正的方式定量;对于超过基质匹配标准曲线最高点浓度的样品,稀释至线性范围内。相关图谱参考附录A。
7.5 空白试验
除不加试料外,采用完全相同的步骤进行平行操作。
8. 试验数据处理
单点校准: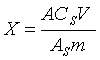
或基质匹配标准曲线校准:由![]() ,求得a和b,则
,求得a和b,则
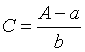
按下式计算阿莫西林的残留量:
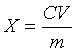
式中:
X——试料中阿莫西林的残留量,µg/kg;
Cs——基质匹配标准溶液中阿莫西林的浓度,ng/mL;
C——试料溶液中阿莫西林的浓度,ng/mL;
As——基质匹配标准溶液中阿莫西林的峰面积;
A——试料溶液中阿莫西林的峰面积;
V——试料最终定容体积,mL;
![]() ——称样量,g。
——称样量,g。
注:计算结果需扣除空白值,测定结果用平行测定的算术平均值表示,保留三位有效数字。
9 检测方法的灵敏度、准确度和精密度
9.1 灵敏度
本方法在牛组织(肾脏、肝脏和脂肪)中阿莫西林的定量限为10µg/kg。
9.2 准确度
本方法牛组织(肾脏、肝脏和脂肪)10~100μg/kg添加浓度水平上的回收率为60.0~110.0%。
9.3 精密度
本方法批内相对标准偏差≤20%,批间相对标准偏差≤20%。
附录 A
(资料性附录)
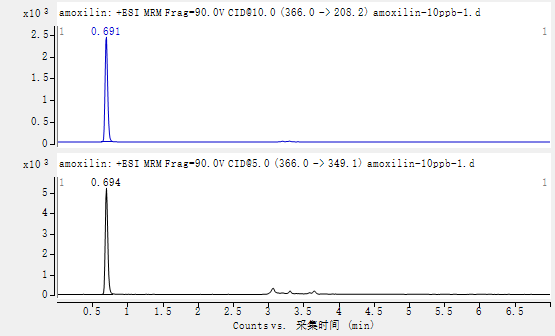
图A1 阿莫西林标准溶液(10ng/mL)特征离子色谱图
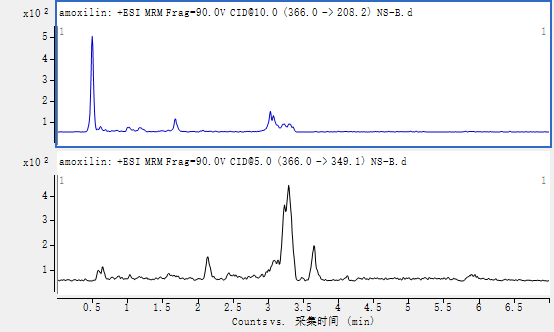
图A2 牛肾脏空白试样溶液特征离子质量色谱图
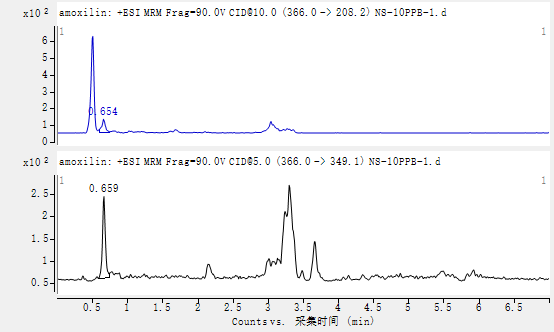
图A3 牛肾脏基质匹配阿莫西林标准溶液特征离子质量色谱图(10μg/kg)
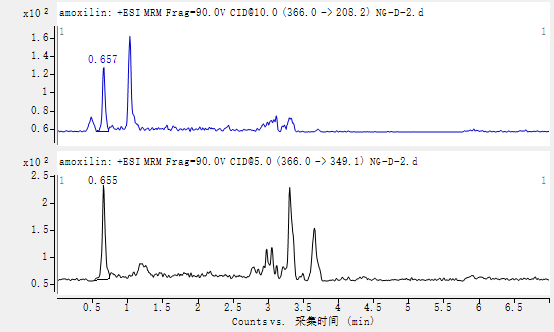
图A4 牛肾脏空白添加试样溶液特征离子质量色谱图(10μg/kg)
附件5
马波沙星的每日允许摄入量和最高残留限量(试行)
申报单位参照欧盟EMA相关标准制定了马波沙星每日允许摄入量(ADI)和马波沙星在牛组织及牛奶中的最高残留限量(MRL),如下表:
|
活性成分 |
残留标志物 |
动物品种 |
靶组织 |
MRLs |
|
马波沙星 ADI: 0~4.5μg/kg b.w./d |
马波沙星 |
牛 |
脂肪 |
50μg·kg-1 |
|
肌肉 |
150μg·kg-1 |
|||
|
肝脏 |
150μg·kg-1 |
|||
|
肾脏 |
150μg·kg-1 |
|||
|
牛奶 |
75μg·kg-1 |
相关新闻
- 中华人民共和国农业农村部公告第469号 2021-12-07
- 中华人民共和国农业农村部公告第474号 2021-12-07
- 中华人民共和国农业农村部公告第355号 2021-01-29
- 中华人民共和国农业农村部公告第344号 2020-12-20
- 中华人民共和国农业农村部公告第322号 2020-11-24



 提示信息
提示信息