中华人民共和国农业农村部公告 第89号
根据《兽药管理条例》和《兽药注册办法》规定,经审查,批准法国诗华动物保健公司生产的马波沙星注射液在我国变更注册,并发布修订后的产品质量标准、说明书和标签以及最高残留限量和残留检测方法标准,自发布之日起执行。此前发布的上述产品兽药质量标准、说明书和标签同时废止。
特此公告。
附件:1.进口兽药注册目录
2.质量标准
3.说明书和标签
4.马波沙星的每日允许摄入量和牛脂肪组织中最高残留限量(试行)
5.牛脂肪组织中马波沙星残留检测方法标准(试行)
农业农村部
2018年11月20日
附件1
进口兽药注册目录
|
兽药名称 |
生产厂名称 |
国 别 |
进口兽药注册证书号 |
有效 期限 |
备注 |
|
马波沙星注射液(50ml:5g) Marbofloxacin Injection |
法国诗华动物保健公司 CEVA SANTE ANIMALE S.A. |
法国 |
(2016)外兽药证字30号 |
2016.07.27- 2021.07.26 |
变更注册:增加靶动物牛 |
|
马波沙星注射液(100ml:10g) Marbofloxacin Injection |
(2016)外兽药证字31号 |
2016.07.27- 2021.07.26 |
|||
|
马波沙星注射液(250ml:25g) Marbofloxacin Injection |
(2016)外兽药证字32号 |
2016.07.27- 2021.07.26 |
附件2(略)
附件3
马波沙星注射液说明书和标签
一、 马波沙星注射液说明书
兽用
【兽药名称】
通用名称:马波沙星注射液
商品名称:牧康欣Ò(Marbox®)
英文名称:Marbofloxacin Injection
汉语拼音:Maboshaxing Zhusheye
【主要成分】马波沙星
【性状】本品为黄色澄明液体。
【药理作用】 药效学 马波沙星是动物专用的氟喹诺酮类抗菌药。主要通过抑制细菌脱氧核糖核酸回旋酶A亚基的活性而抑制细菌DNA复制、转录及蛋白质的合成。马波沙星抗菌谱广,对革兰氏阳性菌(特别是葡萄球菌属)、革兰氏阴性菌(大肠杆菌、多杀性巴斯德杆菌、溶血性曼氏杆菌、睡眠嗜组织菌、鼠伤寒沙门氏菌、空肠弯曲杆菌、费氏柠檬酸杆菌、阴沟肠杆菌、粘质沙雷氏菌、摩氏摩根氏菌、变形杆菌、志贺菌属、猪胸膜肺炎放线杆菌、支气管败血性鲍特氏菌、克雷伯菌属、嗜血杆菌属等)及支原体有效。
药动学 动物注射马波沙星吸收迅速而完全,血浆蛋白结合率低,生物利用度接近100%。猪肌内注射马波沙星2mg/kg,约1小时血药浓度即可达峰值,Cmax约为1.7µg/ml。牛肌内单次注射马波沙星8mg/kg,约1 小时血药浓度可达到峰值,Cmax约8µg/ml;牛皮下注射马波沙星2mg/kg后,约1小时血药浓度可达到峰值,Cmax约1.7 µg/ml。马波沙星广泛分布于肝、肾、皮肤、肺、膀胱等组织,在大部分组织内的药物浓度高于血药浓度。马波沙星在猪体内的消除半衰期为8.7小时,牛肌内注射消除半衰期为9.5小时,牛皮下注射消除半衰期 为5.6小时,主要以原形经尿和粪便排泄。
【适应证】 用于治疗由敏感菌引起的母猪子宫炎-乳腺炎-无乳综合征,牛呼吸道感染和牛泌乳期乳腺炎。
【用法与用量】 以马波沙星计。
母猪子宫炎-乳腺炎-无乳综合征:肌内注射。一次量,每1kg体重2mg(即每50kg体重1ml),一日1次,连用3日。
牛呼吸道感染:肌内注射。一次量,每1 kg体重8mg(即每25kg体重2ml),单次注射。同一部位使用不得超过20ml。
牛泌乳期乳腺炎:皮下注射。一次量,每1kg体重 2mg(即每50kg体重1ml),一日1次,连用3日。
【不良反应】 本品可能会引起注射部位短暂的刺激反应。
【注意事项】
1.仅在兽医指导下使用。
2. 猪、牛推荐颈部肌内注射。
3. 对马波沙星或其他喹诺酮类药物过敏的动物禁用。
4. 已知对喹诺酮类药物耐药的菌株或疑似耐药菌株感染的动物禁用。
5. 对喹诺酮类药物过敏的人员避免接触本品。
6. 如果不慎与皮肤或眼睛接触,立即用大量水进行冲洗。
7. 瓶塞最多可穿刺45次,应选择合适的包装规格。
【休药期】 猪4日;牛肌内注射3日,弃奶期72小时;牛皮下注射6日,弃奶期36小时。
【规格】 按C17H19FN4O4计算 (1)50ml:5g (2)100ml:10g (3)250 ml:25g
【包装】
【贮藏】 遮光,密闭保存。
【有效期】 36个月;开启后28日。
【进口兽药注册证号】
【生产企业】 法国诗华动物保健公司(CEVA SANTE ANIMALE S.A.)
地址:10 AVENUE DE LA BALLASTIERE,33500 LIBOURNE,FRANCE
二、 马波沙星注射液标签
兽用
【兽药名称】
通用名称:马波沙星注射液
商品名称:牧康欣Ò(MarboxÒ)
英文名称:Marbofloxacin Injection
汉语拼音:Maboshaxing Zhusheye
【主要成分】 马波沙星
【性状】 本品为黄色澄明液体。
【适应证】 用于治疗由敏感菌引起的母猪子宫炎-乳腺炎-无乳综合征,牛呼吸道感染和牛泌乳期乳腺炎。
【用法与用量】 以马波沙星计。
母猪子宫炎-乳腺炎-无乳综合征:肌内注射。一次量,每1kg体重2mg(即每50kg体重1ml),一日1次,连用3日。
牛呼吸道感染:肌内注射。一次量,每1kg体重8mg(即每25kg体重2ml),单次注射。同一部位使用不得超过20 ml。
牛泌乳期乳腺炎:皮下注射。一次量,每1kg体重 2mg(即每50kg体重1ml),一日1次,连用3日。
【休药期】 猪4日;牛肌内注射3日,弃奶期72 小时;牛皮下注射6日,弃奶期36 小时。
【规格】 按C17H19FN4O4计算 (1)50ml :5g (2)100ml :10g (3)250ml :25g
【包装】
【生产日期】
【生产批号】
【有效期】至
【贮藏】 遮光,密闭保存。
【进口兽药注册证号】
【生产企业】 法国诗华动物保健公司(CEVA SANTE ANIMALE S.A.)
地址:10 AVENUE DE LA BALLASTIERE, 33500 LIBOURNE, FRANCE
附件4
马波沙星的每日允许摄入量和牛脂肪组织中最高残留限量(试行)
参照欧盟EMA相关标准中马波沙星每日允许摄入量(ADI)以及在牛脂肪组织中最高残留限量(MRL),申报单位制定马波沙星在牛脂肪中的最高残留限量(MRL)为50 μg/kg。具体数据见表1。
表1 马波沙星的ADI及在牛脂肪中MRL信息表
|
活性成分 |
残留标示物 |
动物品种 |
靶组织 |
MRL |
|
马波沙星 ADI: 4.5 μg.(kg b.w.)-1 |
马波沙星 |
牛 |
脂肪 |
50μg·kg-1 |
附件5
牛脂肪组织中马波沙星残留检测方法标准(试行)
牛脂肪组织中马波沙星残留量的测定
液相色谱-串联质谱法(试行)
1 范围
本标准规定了牛脂肪组织中马波沙星残留量检测的制样和液相色谱-串联质谱(LC-MS)测定方法。
本标准适用于牛脂肪组织中马波沙星残留的定性和定量测定。
2 规范性引用文件
下列文件中的条款通过本标准的引用而成为本标准的条款。凡是注日期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用于本标准,然而,鼓励根据本标准达成协议的各方研究是否可使用这些文件的最新版本。凡是不注日期的引用文件,其最新版本适用于本标准。
GB/T 6379 测试方法的精密度 通过实验室间试验确定标准测试方法的重复性和再现性
GB/T 1.1-2009 标准化工作导则 第1部分:标准的结构和编写规则
GB/T 6682 分析实验室用水规则和试验方法
3 制样
3.1 样品的制备
取新鲜或解冻的空白或供试动物组织,剪碎,并使均质。
3.2 样品的保存
-20℃以下保存。
4 测定方法
4.1 方法提要或原理
牛脂肪中残留的马波沙星用5%三氯乙酸溶液(TCA)和含1%乙酸的乙腈溶液提取(V/V=8∶2),正己烷除脂,以马波沙星-D8为内标,用液相色谱-串联质谱法测定,内标法定量。
4.2 试剂和材料
以下所用的试剂,除特别注明者外均为分析纯试剂;水为符合GB/T 6682规定的一级水。
4.2.1 马波沙星对照品:含量≥98.0%。
4.2.2 马波沙星-D8对照品:含量≥98%。
4.2.3 甲醇:色谱纯。
4.2.4 甲酸铵:色谱纯。
4.2.5 甲酸:色谱纯。
4.2.6 乙酸。
4.2.7 三氯乙酸(TCA)。
4.2.8 二甲基亚砜。
4.2.9 正己烷。
4.2.10 1mol/L甲酸铵溶液
称取3.15g甲酸铵,置50ml容量瓶中,用水溶解并稀释至刻度。
4.2.11 5%三氯乙酸(TCA)
称取50.0g三氯乙酸,置1000ml容量瓶中,用水溶解并稀释至刻度。
4.2.12 含1%乙酸的乙腈溶液
量取500ml乙腈和10ml乙酸,置1000ml容量瓶中,混匀,用乙腈稀释至刻度。
4.2.13 马波沙星标准储备液(1000µg/ml)
取马波沙星对照品约10mg,精密称定,置10ml容量瓶中,用二甲基亚砜溶解并稀释至刻度,配制成为浓度为1000µg/ml的马波沙星标准储备液。-18 ℃以下保存,有效期6个月。
4.2.14 马波沙星-D8内标储备液(100µg/ml)
取马波沙星-D8对照品0.5mg,精密称定,置5ml容量瓶中,用二甲基亚砜溶解并稀释至刻度,配制成浓度为100µg /ml的马波沙星-D8内标储备液。-18 ℃以下保存,有效期6个月。
4.2.15 马波沙星标准工作液(2μg/ml)
精密量取马波沙星标准储备液适量,用乙腈稀释成浓度为2μg/ml的标准工作液。现用现配。
4.2.16 马波沙星-D8内标工作液(1.2μg/ml)
精密量取马波沙星-D8内标储备液适量,用乙腈稀释成浓度为1.2μg/ml的内标工作液。现用现配。
4.3 仪器和设备
4.3.1 液相色谱-串联质谱仪:配有电喷雾离子源。
4.3.2 分析天平:感量0.00001g;感量0.0001g。
4.3.3 天平:感量0.01g。
4.3.4 匀浆机。
4.3.5 离心机。
4.3.6 涡旋混合器。
4.3.7 离心管:50ml。
4.3.8 试管:10ml。
4.3.9 棕色容量瓶:5ml,50ml,100 ml。
4.3.10滤膜:0.22μm。
4.4 测定步骤
4.4.1试样的制备
取新鲜或冷冻空白或供试组织,剪碎,并使均质。
——取均质后的供试样品,作为供试试样。
——取均质后的空白样品,作为空白试样。
——取均质后的空白样品,添加适宜浓度的标准工作液,作为空白添加试样。
4.4.2试样保存
-20℃以下保存。
4.4.3 提取
称取试样(2 ± 0.01)g,置50 ml离心管中,添加1.2μg/ml马波沙星-D8内标工作液适量,加5%TCA溶液和含1%乙酸的乙腈溶液(V/V=8∶2)5ml,振荡5min, 10000r/min 离心10min,取上清液1.5ml于10ml试管中,加正己烷2ml,涡旋1min,静置5min,取下层清液1ml,滤膜过滤,供液相色谱-串联质谱分析测定。
4.4.4 标准曲线的制备
精密量取2μg/ml马波沙星标准工作液和1.2μg/ml马波沙星-D8内标工作液适量,用空白脂肪提取液稀释,配制成马波沙星-D8浓度均为120ng/ml以及马波沙星浓度为6、10、20、80、160、200、340和400ng/ml的系列标准工作液,供液相色谱-串联质谱分析测定。以马波沙星特征离子质量色谱峰面积与内标物峰面积比值为纵坐标,以马波沙星浓度为横坐标,绘制标准曲线。计算回归方程和相关系数。
4.4.5 测定
4.4.5.1 液相色谱条件
色谱柱:C18 柱 (2.0 mm×150 mm,粒径5μm), 或效能相当者;
流动相:流动相A为1000ml水+1ml甲酸+500μl 1mol/L甲酸铵溶液;流动相B为1000ml甲醇+1ml甲酸+500μl 1mol/L甲酸铵溶液,梯度洗脱条件参见表2;
流速:0.25 ml/min;
柱温:30℃;
进样量:5μl。
表2 梯度洗脱条件
|
时间/min |
A/% |
B/% |
|
0 |
90 |
10 |
|
6 |
10 |
90 |
|
10 |
10 |
90 |
|
11 |
30 |
70 |
|
12 |
90 |
10 |
|
18 |
90 |
10 |
4.4.5.2 质谱条件
离子源:电喷雾离子源;
扫描方式:正离子扫描;
检测方式:多反应监测;
气体温度:350℃;
辅助气:N2;
辅助气流速:9.0L/min。
目标化合物定性、定量离子对、去簇电压和碰撞能量见表3。
表3 目标化合物定性、定量离子对、去簇电压和碰撞能量
|
目标化合物 |
定性离子对m/z |
定量离子对m/z |
去簇电压(V) |
碰撞能量(eV) |
|
马波沙星 |
363.1>320.1 |
363.1>345.1 |
115 |
12 |
|
363.1>345.1 |
16 |
|||
|
马波沙星-D8 |
370.1>328.2 |
370.1>328.2 |
105 |
12 |
4.4.5.3 测定法
4.4.5.3.1 定性测定
通过试样色谱图的保留时间与相应标准溶液的保留时间、各色谱峰的特征离子与相应浓度标准溶液各色谱峰的特征离子相对照定性。试样与标准溶液保留时间的相对偏差不大于5%;试样特征离子的相对丰度与浓度相当标准溶液的相对丰度一致,相对丰度偏差不超过表4的规定,则可判断试样中存在相应的被测物。
表4 定性测定时相对离子丰度的最大允许偏差
|
相对离子丰度 |
>50% |
>20%至50% |
>10%至20% |
≤10% |
|
允许的相对偏差 |
±20% |
±25% |
±30% |
±50% |
4.4.5.3.2 定量测定
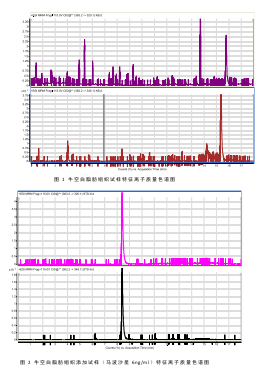
取试样溶液和标准溶液,做单点或多点校准。按内标法以峰面积比定量。标准溶液及试样溶液中的马波沙星响应值均在仪器检测的线性范围内。在上述色谱-质谱条件下,马波沙星标准溶液和空白添加试样溶液中特征离子质量色谱图见附录A。
4.4.6 空白实验
除不加试样外,采用完全相同的步骤进行平行操作。
4.5 结果计算和表述
4.5.1 单点校正法
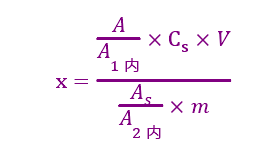
式中:
X为试样中马波沙星的残留量(μg/kg);
A为试样溶液中马波沙星峰面积;
As为标准溶液中马波沙星峰面积;
A1内为试样溶液中内标物峰面积;
A2内为标准溶液中内标物峰面积;
Cs为标准溶液中马波沙星浓度(ng/ml);
V为试样最终定容体积(ml);
m为试样的质量(g)。
注:计算结果需要扣除空白值,测定结果用平行测定的算术平均值表示,保留三位有效数字。
4.5.2 多点校正法
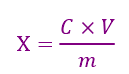
式中:
X为试样中马波沙星的残留量(μg/kg);
C为根据标准曲线计算得到的试样中马波沙星的浓度(ng/ml);
V为试样最终定容体积(ml);
m为试样质量(g)。
注:计算结果需要扣除空白值,测定结果用平行测定的算术平均值表示,保留三位有效数字。
5方法灵敏度、准确度和精密度
5.1 灵敏度
本方法检出限为7.5μg/kg,定量限为25μg/kg。
5.2 准确度
本方法在25μg/kg~100 μg/kg添加浓度水平上的回收率为80%~120%。
5.3 精密度
本方法的批内相对标准偏差≤20%,批间相对标准偏差≤20%。
附录A
(资料性附录)